2021年6月23~26日,全球肝脏病学领域最具影响力的欧洲肝脏研究协会(EASL)年会—国际肝病大会(ILC 2021)以线上会议的形式举行。本次会议上,中山大学肿瘤防治中心肝脏外科的徐立教授代表陈敏山教授团队口头报告了该中心一项研究者发起的Ⅱ期研究的初步结果。该研究将肝动脉灌注化疗(HAIC)联合PD-1抑制剂信迪利单抗治疗用于局部晚期、潜在可切除肝细胞癌(HCC)的转化治疗,显示出令人鼓舞的疗效,有望为局部晚期HCC患者提供更多治愈机会。作为首个在国际大会上口头汇报的晚期肝癌转化治疗的前瞻性研究,也是本次ILC大会肝癌领域唯一进行口头报告的中国团队,该研究引起了广泛关注,还受主办方EASL邀请参加了本次大会的新闻发布会,专门对研究内容进行重点推介。
研究介绍
肝癌(HCC)恶性度高,预后差,近半数发生于中国,大多数患者初诊时即处于晚期。在西方指南中, 对于伴血管侵犯的晚期HCC患者并不推荐性手术切除,而在中国指南中,手术切除是治疗选择之一,文献报道显示特定患者可从手术切除中获得长期生存。如何提高手术切除率和降低术后复发率成为当前研究热点。本中心以往的系列研究均显示使用FOLFOX方案的HAIC在大肝癌患者中缩瘤效果优于传统TACE,手术转化率更高。而免疫治疗可诱导持久的抗肿瘤反应。因此,研究团队拟通过FOLFOX-HAIC联合PD-1抑制剂,以期达到既高效又持久的转化效果,提高局部晚期潜在可切除HCC患者的无进展生存期。
研究入组30例初诊肝癌患者,治疗前经穿刺病理证实为HCC,主要入组标准包括:肿瘤局限于半肝,伴门静脉癌栓(Vp1-Vp3)和/或肝静脉侵犯,无肝外转移,KPS评分≥90,Child-Pugh A级。主要研究终点为按RECIST 1.1评估的无进展生存期(PFS,定义为首次治疗至疾病进展或术后复发或死亡的时间,以先发生者为准)。次要终点包括客观缓解率(ORR)、疾病控制率(DCR)、手术转化率、总生存(OS)、安全性等。患者接受信迪利单抗 200mg IV D1 + FOLFOX-HAIC D2-3 Q3W治疗,每2周期评估,如果达到PR或SD伴肿瘤明显缩小,MDT评估后实施转化手术,术后接受信迪利单抗单药200mg IV Q3W辅助治疗直至复发或不可耐受毒性,信迪利单抗最多用药16次。未成功转化手术的患者,则继续接受FOLFOX-HAIC及信迪利单抗的联合治疗(最多8个疗程),直至疾病进展或不可耐受毒性。患者出现影像学证实的疾病进展前不接受方案以外的其他抗癌治疗,所有患者随访至死亡。

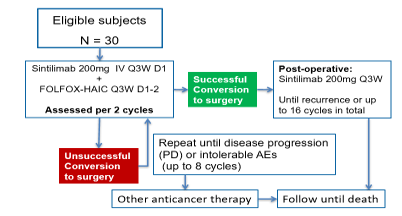
图1. 研究设计
除1例患者自行退出研究外,29例患者接受了疗效评价。截至2021年5月,中位随访时间17.8个月,全组患者中位PFS 15.7个月,12个月PFS率57.9%。亚组分析显示是否进行转化手术对预后有显著影响,未手术和手术患者的中位PFS分别是5.49个月和未达到(P=0.009),手术患者的中位PFS估计可达到24个月以上(图2)。术前ORR为44.8%,DCR 82.7%(图3)。21例成功转化的患者大多在术前仅接受了2周期的联合治疗,成功转化率达72.4%(21/29),其中19例(65.5%)患者接受肝切除术,有3例(15.8%)术后病理完全缓解(pCR),另外2例患者接受射频消融(RFA)治疗(图4)。

图2. PFS

图3. ORR和DCR

图4. 成功转化患者的术前治疗和生存状态
30例患者均纳入安全性评价,27例(90.0%)患者发生至少1次治疗相关不良事件(TRAE),最常见的TRAE为皮肤反应、转氨酶升高和骨髓抑制,大多为1~2级,3~4级TRAE发生率13.3%。仅1例患者出现治疗相关SAE(4级术后肝功能不全),该患者永久终止研究药物治疗,经治疗后肝功能好转。其余患者均完成方案规定的治疗,依从性好,无围手术期或治疗相关死亡。
当前的研究显示FOLFOX-HAIC联合信迪利单抗手术转化率高,接受转化手术后的患者具有出色的PFS,且安全性可控。该联合治疗策略可考虑作为局部晚期HCC转化治疗的优选方案。目前研究还在继续进行中,期待未来更多的数据披露。
HCC预后不佳,手术切除是早期HCC患者首选的治疗方法,可使患者获得长期生存。然而HCC起病隐匿,大多数患者就诊时已经处于局部晚期或转移,丧失手术机会。既往报道40%~60%的HCC侵犯肝脏大血管系统,尤其是门静脉系统,此类患者中位生存期常不足1年。针对这部分患者目前东西方治疗差异大,国外指南普遍推荐药物系统治疗,但国内指南多推荐MDT治疗,手术切除推荐用于部分患者。既往研究显示R0切除能够提高局晚期HCC患者的生存时间。因此,使用新型治疗方案积极进行转化治疗提高手术切除率,可能可为患者带来生存获益。近年来随着免疫治疗和靶向治疗的快速发展,HCC的系统治疗迎来了全新治疗模式,PD-1/PD-L1抑制剂联合抗血管生成治疗已经成为晚期HCC患者的优选一线治疗方案。而免疫治疗和局部治疗相结合的手段也成为新的研究热点,有望为中晚期HCC患者的转化治疗增添一抹亮色。
这项研究显示信迪利单抗+FOLFOX-HAIC的术前ORR达到44.8%,DCR 82.7%,转化切除率高达65.5%,其中15.8%达到pCR。长期随访数据显示全组患者中位PFS达到15.7个月,特别是接受手术治疗的患者,中位PFS预计超过24个月,治愈的可能大大增加。患者的OS数据还将进一步随访。作为第一个在国际大会上口头汇报的晚期肝癌转化治疗的前瞻性研究,该研究显示出极具潜力的初步结果,和历史数据相比极大改善了此类患者的预后,有望为局部晚期肝癌患者开创新的治疗模式,因此也引起了西方学者的关注,将该研究在大会新闻发布会环节进行重点推介。
HCC的转化治疗已成为目前关注的焦点,然而研究数据相对较少,最佳治疗方式仍未可知,还需更多高级别临床证据支持。这项研究有力补充了转化治疗的数据,并证实PD-1抑制剂联合HAIC是一种令人鼓舞的治疗方式。然而,肝癌转化治疗仍然存在很多挑战,包括手术时机的确定,方案对于术后复发的作用,患者的长期生存情况,获益人群的预测生物标志物等。这些问题都有待进一步的随访来持续探索。研究证实,PD-1抑制剂信迪利单抗联合HAIC可作为局部晚期HCC的有效转化治疗方案,转化率高,可改善患者无进展生存,且安全性良好。期待该方案为更多HCC患者带来治愈希望。
中山大学肿瘤防治中心肝脏外科 主任医师
医学博士,博士研究生导师
美国约翰霍普金斯大学博士后
广东省杰出青年医学人才
中国抗癌协会肝癌专业委员会青年委员会副主任委员
国家癌症中心肝癌质控专家委员会委员
广东省医学会肝癌分会副主任委员
中华医学会肝病学分会肝癌学组委员
国际肝胆胰协会中国分会肝胆胰MDT专业委员会委员
广东省抗癌协会肝癌专业委员会常委兼秘书
获广东省科学技术奖一等奖、教育部科技进步奖二等奖等





 京公网安备 11010502033352号
京公网安备 11010502033352号